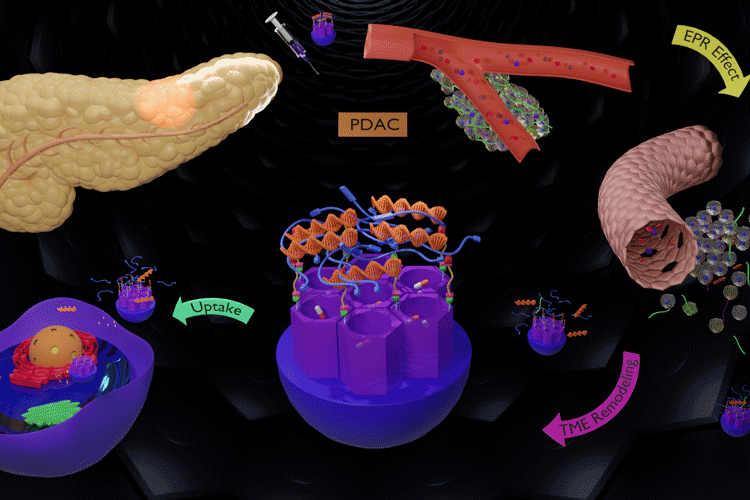
El càncer de pàncrees representa la quarta causa de mort relacionada amb càncer a Europa i als Estats Units. La seva forma més comuna és l’adenocarcinoma ductal pancreàtic (PDAC), asimptomàtic fins a estadis ben avançats de la malaltia, i que va representar el tercer càncer més mortal el 2023. Els tractaments actuals, basats en la quimioteràpia, presenten una baixa eficàcia deguda, en part, a la formació d’un estroma altament fibròtic que aïlla les cèl·lules tumorals i incrementa la pressió intersticial. Això dificulta l’arribada dels fàrmacs i afavoreix el desenvolupament de resistències.
Actualment, la nanomedicina és una disciplina innovadora i d’avantguarda capaç de millorar la farmacodinàmica dels principis actius. Durant l’última dècada, els nanovehicles han guanyat rellevància en l’abordatge terapèutic del PDAC. Tot i la seva capacitat per millorar la selectivitat dels fàrmacs envers les cèl·lules malignes i permetre una alliberació controlada, una de les principals limitacions dels nanosistemes és la formació immediata d’una corona proteica (PC) a la seva superfície tan bon punt són injectats al torrent sanguini. Aquestes proteïnes adherides a la superfície de les partícules actuen com una etiqueta que facilita que les cèl·lules del sistema immunitari les detectin i eliminin ràpidament, disminuint l’acumulació selectiva dels sistemes al lloc diana.
En aquest context, la Dra. Iris Ponton Barroso ha dut a terme la seva tesi doctoral a IQS amb l’objectiu de desenvolupar i estudiar nous nano-vehicles basats en nanopartícules mesoporoses de silice (MSN) capaços de superar els desafiaments del PDAC. Sota el títol Engineering Artificial Protein Coronas on Mesoporous Silica Nanoparticles: A Targeted Approach for Pancreatic Cancer Therapy, la tesi ha estat dirigida pel Dr. David Sánchez Garcia, dins del Grup d’Enginyeria de Materials – GEMAT d’IQS.
A la seva tesi, la Dra. Pontón proposa tres nanosistemes basats en MSNs per superar els desafiaments associats al PDAC, tot abordant el problema de la formació de PCs al voltant de les nanopartícules (NPs). Per fer això, les NPs han estat funcionalitzades amb una corona d’albúmina, per reduir la seva detecció pels macròfags, que, a més, actua com a tap per retenir els fàrmacs dins les NPs. La unió de l’albúmina a les NPs s’ha dut a terme mitjançant noves molècules dissenyades i sintetitzades al Laboratori de Química Supramolecular. Aquestes molècules, que tenen grups sensibles a estímuls concrets, han permès la preparació de nous sistemes d’alliberament controlat.
Nous nanovehicles amb una corona artificial per l’alliberament controlat de fàrmacs
El primer sistema consisteix en un nanovehicle format per MSNs i una corona d’albúmina, capaç d’alliberar de manera controlada un conjugat de camptotecina i gemcitabina (CPT-GEM) en resposta al pH àcid dels lisosomes de les cèl·lules tumorals. A més s’han afegit a la corona proteica dos pèptids per donar selectivitat al sistema per les cèl·lules de PDAC i reduir encara més el segrest dels sistemes pels macròfags. Aquest sistema s’ha avaluat en cèl·lules de PDAC, mostrant una eficàcia superior a la dels sistemes anàlegs descrits a la literatura basats en monoteràpia amb gemcitabina.
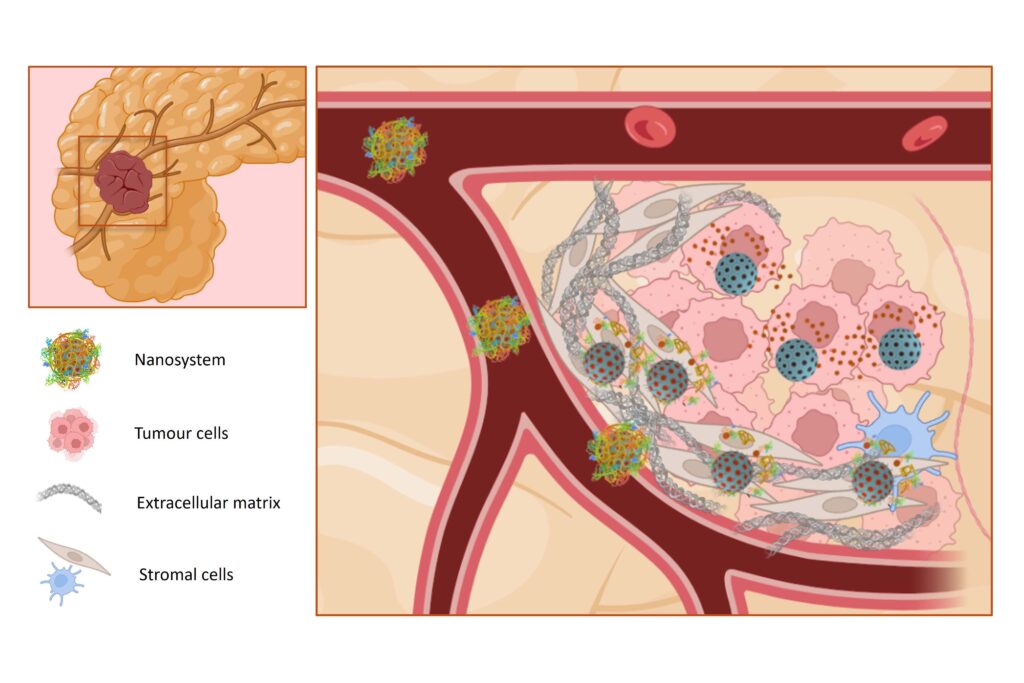
La segona proposta tenia com a objectiu preparar i caracteritzar un nanovehicle que combina la teràpia fotodinàmica i quimioteràpia. El disseny d’una corona proteica sensible a l’oxigen singlet va permetre obtenir un sistema d’alliberament controlat del fàrmac doxorubicina mitjançant llum. Aquest sistema ha mostrat una elevada citotoxicitat a concentracions molt baixes del nanovehicle quan és irradiat amb llum vermella.
El tercer nanovehicle desenvolupat en aquesta tesi tenia com a objectiu crear un sistema avançat potencialment capaç tant d’acumular-se en el microambient tumoral del càncer de pàncrees, com de penetrar-hi. Per aconseguir-ho, es van utilitzar NPs de 45 nm de diàmetre carregades amb el fàrmac conjugat CPT-GEM. Els nanovehicles es van conjugar amb un recobriment híbrid format per un polímer catiònic i albúmina, units a les NPs mitjançant una nova molècula amb dos grups sensibles a dos pHs. Gràcies a aquests estímuls, aquesta estratègia permet reduir progressivament la mida del tumor en el medi extracel·lular i a l’interior de les cèl·lules tumorals. Aquest, nanovehicle ha mostrat una eficàcia, front dues línies cel·lulars de PDAC, superior a la dels sistemes anàlegs descrits a la literatura basats en monoteràpia amb gemcitabina. Tant el disseny com els resultats obtinguts amb aquest sistema, el proveeixen amb potencial per a l’avaluació preclínica.
Part d’aquesta recerca s’ha realitzat en col·laboració amb el Laboratori d’Enginyeria de Teixits i el Laboratori de Bioteràpies d’IQS.
Publicacions relacionades
Preparation of porphyrin and phthalocyanine conjugates for biomedical applications, 2021, Journal of Porphyrins and Phthalocyanines, 25, 917-929
Preparation and Applications of Organo-Silica Hybrid Mesoporous Silica Nanoparticles for the Co-Delivery of Drugs and Nucleic Acids, Nanomaterials 2020, 10(12), 2466
Part d’aquesta tesi s’ha dut a terme amb ajut del Ministerio de Ciencia e Innovación – AEI en el marc del projecte Nanopan-3D (PID2021-126346OB-I00).